Focus L’Essentiel B22 / Recherche
Faire repousser les dents en 2025 ? Mythe ou réalité ?
Accueil > Actualités > Focus séance B22 – Faire repousser les dents en 2025 ? Mythe ou réalité ?
Mercredi 26 novembre – 11h-12h
Responsable scientifique : Anne Poliard
Conférenciers : Ariane Berdal
Des campagnes médiatiques annoncent le démarrage d’essais cliniques du « premier médicament de régénération dentaire » dans l’hôpital universitaire de Kyoto au Japon (Pr. Katsu Takahashi). Le médicament qui sera injecté par voie sanguine est un anticorps désactivant USAG-1, une protéine inhibitrice de plusieurs voies moléculaires de l’odontogenèse. Le premier objectif est de traiter des patients atteints de maladies rares, porteurs d’agénésies dentaires multiples (informations : www.tetecou.fr). Le deuxième objectif vise le patient « ordinaire », (pertes dues à une carie, la maladie parodontale ou un trauma). Le médicament stimulerait la pousse d’une troisième génération de germes dentaires, présente dans les mâchoires humaines mais silencieuse, bloquée dans son développement. S’il est bien établi que l’être humain ne possède que deux dentitions (une temporaire et une permanente), plusieurs études histologiques ont observé l’apparition transitoire de bourgeons supplémentaires, comparables à des germes d’une troisième dentition. Ces structures régressent rapidement et ne donnent pas naissance à des dents fonctionnelles dans des conditions normales. Cependant, dans certaines situations pathologiques ou génétiques, cette « troisième dentition » pourrait être réactivée et conduire à l’apparition de dents surnuméraires. Ce phénomène suscite aujourd’hui un intérêt croissant en recherche fondamentale et clinique.
La vraie vie des essais cliniques de régénération dentaire :
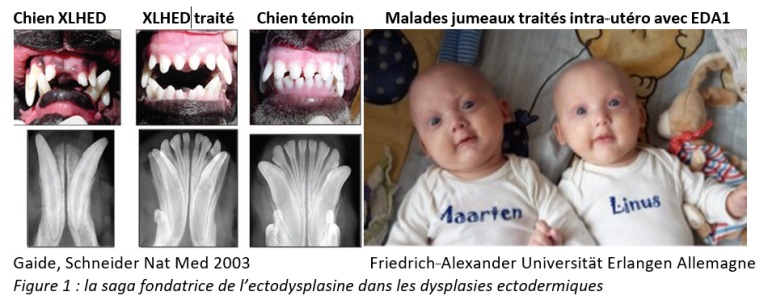
Des stratégies de régénération dentaire notamment celle utilisant l’ectodysplasine pour les agénésies dentaires des dysplasies ectodermiques sont conduites depuis plusieurs années [1-4]. Les essais cliniques ont suivi les travaux sur modèles animaux (exemple : chien XLHED porteur du gène non fonctionnel de l’ectodysplasine : Figure 1). Les études cliniques de phase I ont établi l’innocuité du médicament. Les études pilotes de phase II chez les malades ont montré que l’injection anténatale du médicament (Figure 1) était requise, les traitements postnataux s’avérant d’un impact modéré [4].
En anténatal, des essais internationaux de phase II « EDELIFE » sont en cours [5]. Ce consortium n’a pas eu une couverture médiatique de l’ampleur de celle d’USAG-1 alors que l’ectodysplasine ER004 guérirait en plus des dents, cheveux, poils, glandes sudoripares, poumons, sauvant dans les formes les plus graves de la maladie les enfants d’une mort probable ou d’un handicap majeur pour le restant de leur vie. En effet, les voies moléculaires de l’odontogenèse sont opérationnelles dans de nombreux autres organes : peau, os, intestin, cœur, œil, cerveau et dans certains cancers. Apporter une molécule normale pour remplacer la molécule déficiente résultant du variant génétique pathogène est spécifique. Il cible les cellules répondantes et corrige leur défaut.
Correction des agénésies dentaires par l’anticorps USAG-1 : anti-USAG
Les agénésies dentaires correspondent non pas à une absence de germes dentaires mais au blocage précoce de leur morphogenèse (bourgeons émanant de la lame dentaire). La protéine USAG-1 est un inhibiteur avéré de deux voies cardinales du développement dentaire, Wnt et BMP [6-7]. Ces molécules sont au cœur des communications cellulaires de nombreux organes tout au long de la vie, de l’embryon à l’âge adulte – dans les cellules-souches et cancéreuses notamment. Bloquer leur inhibiteur par l’anticorps anti-USAG revient à activer ces puissants facteurs de croissance, ce qui a permis de redémarrer le programme dentaire de germes bloqués par plusieurs maladies génétiques en expérimentation animale [6-8].
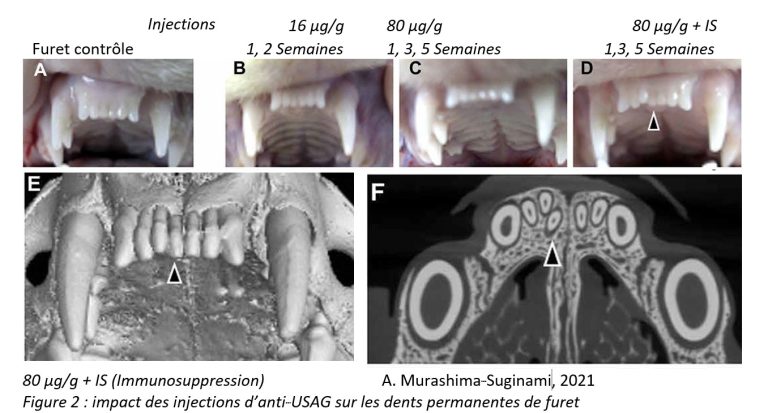
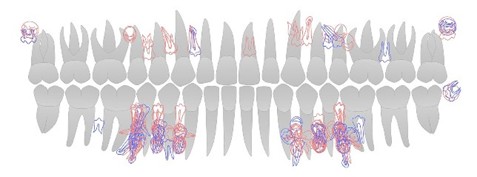
De plus, chez le furet normal qui est comme nous porteur de deux dentitions, une dent surnuméraire a été obtenue par injection d’anti-USAG (Figure 2 [6]). L’équipe japonaise envisage ainsi l’existence d’une troisième génération dentaire silencieuse chez l’adulte dans notre espèce, qui permettrait la génération de dents surnuméraires [9]. Une recherche détaillée [10] sur cette troisième génération localise les dents-candidates dans différents secteurs chez les hommes (bleu) et les femmes (rouge).

Figure 3 : Evaluation de la troisième dentition (dents surnuméraires tardives) [10]
Le chemin de la thérapeutique anti-USAG suit, comme l’ectodysplasine l’a fait auparavant, ce long parcours des phases I et II, cette dernière en deux étapes-clés : la première chez les patients génétiquement atteints d’agénésies dentaires multiples, puis la deuxième chez les patients qui ont perdu leurs dents pour des motifs infectieux ou traumatique, en bref nos patients ordinaires. Dans l’état actuel de la recherche, ces thérapies si elles fonctionnent sans effets secondaires ne seraient valables que pour traiter des enfants porteurs d’une des mutations de gènes affectant l’émergence des bourgeons. Ce type de traitement n’est pas valable chez l’adulte « ordinaire » et ne va pas permettre de faire repousser des dents pour lesquels les traitements actuels restent les seuls que l’on peut proposer.
La régénération dentaire est décrite comme un marché à fort potentiel financier (Fort Collins, Colorado, May 11, 2024 – GLOBE NEWSWIRE). Evalué à 4,04 milliards US Dollars en 2023, il est projeté atteindre 6,28 milliards en 2030, ce qui correspond à un taux de croissance annuel exceptionnel. Ceci résulte de la prévalence des maladies dentaires, des progrès technologiques et du changement de la demande des patients vers des solutions naturelles régénératives. Dans les dynamiques sociétale et économique entourant ces innovations, la diversité culturelle est intéressante. Le médicament ectodysplasine découvert en Suisse a dû passer dans une entreprise américaine financée sur capital risque de par la timidité des investisseurs européens. Il a dû revenir sur notre continent par la non rentabilité inhérente à la lenteur du projet qui a dégouté les investisseurs et est soutenu aujourd’hui sur des fonds Européens. L’investissement du Japon pour le projet USAG-1 est colossal et s’accompagne de campagnes médiatiques tout aussi significatives. L’enjeu de la régénération dentaire est de taille. Ces informations sont enthousiasmantes, la restauration ad integrum étant l’objectif des odontologistes en lieu et place de dispositifs médicaux par définition imparfaits.
Il faut soutenir la recherche pour progresser, innover, avancer, découvrir.
Suivre les expérimentations permet de dispenser les soins conformément aux données actuelles de la science.
On pourrait conclure : la science avance « allegro ma non tropo ».
La dent biologique devrait être pour … après-demain. On y travaille !
Bbliographie
- Gaide, O.; Schneider, P. Permanent correction of an inherited ectodermal dysplasia with recombinant EDA. Nat. Med. 2003, 9,614–618.
- Casal, M.L.; Lewis, J.R.; Mauldin, E.A.; Tardivel, A.; Ingold, K.; Favre, M.; Paradies, F.; Demotz, S.; Gaide, O.; Schneider, P. Significant correction of disease after postnatal administration of recombinant ectodysplasin A in canine X-linked ectodermal dysplasia. Am. J. Hum. Genet. 2007, 81, 1050–1056.
- Schneider,H et al. Prenatal correction of X-linked hypohidrotic ectodermal dysplasia. N. Engl. J.Med. 2018, 378, 1604–1610.
- Schneider, H. Ectodermal dysplasias: New perspectives on the treatment of so far immedicable genetic disorders. Front. Genet. 2022, 13, 1000744.
- Schneider, H.; Hadj-Rabia, S et al. Protocol for the phase 2 EDELIFE trial investigating the efficacy and safety of intra-amniotic ER004 administration to male subjects with X-linked hypohidrotic ectodermal dysplasia. Genes 2023, 14, 153.
- Murashima-Suginami A, et al. Anti-USAG-1 therapy for tooth regeneration through enhanced BMP signaling. Sci Adv. 2021 Feb 12;7(7):eabf1798.
- Takahashi K, et al.. Development of a new antibody drug to treat congenital tooth agenesis. J Oral Biosci. 2024 Dec;66(4):1-9.
- Ravi V, et al. Advances in tooth agenesis and tooth regeneration. Regen Ther. 2023 Feb 3;22:160-168.
- H. Kiso, K. Takahashi, S. et al. , Third dentition is the main cause of premolar supernumerary tooth formation. J. Dent. Res. 98, 968–974 (2019).
- Li X, Gong X, Yu M, Gao X Clinical features of non-syndromic late developing supernumerary teeth : a sign of the third dentition ?. BMC Oral Health. 2024 Mar 28;24(1):397.
Faire repousser les dents en 2025 ? Mythe ou réalité ?
Séance L’Essentiel B22
Mercredi 26 novembre – 11h-12h




